
"Nieszczelność" mitochondriów a długość życia
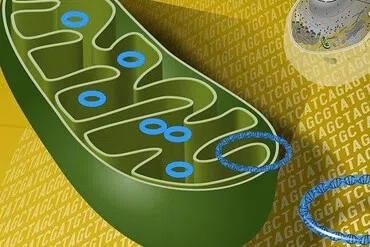


Mitochondria to takie małe-wielkie organelle komórkowe, które pełnią rolę silniczków i filterków naszego organizmu. Znajdują się w każdej komórce, w każdej tkance. Mamy je w skórze, mięśniach, sercu, wątrobie, wszędzie. By komórka była zdrowa musi mieć dobrze funkcjonujące mitochondrium. Jeśli mitochondrium źle funkcjonuje, komórka też podupada na zdrowiu, a jeśli takich chorych komórek jest obok siebie więcej – choroba rozlewa się na tkankę, organ.
Chorująca tkanka, organ wiedzie nas najczęściej do lekarza. A wszystko zaczęło się w mitochondrium, które ma rozmiary od 2 do 9 μm.
Naukowcy z Massachusetts General Hospital, USA sprawdzali jakie znaczenie ma przepuszczalność mitochondriów dla starzenia się organizmu i jego zdrowia. Interesowała ich autofagia, czyli proces, w którym mitochondrium, pozbywa się zbędnej zawartości, usuwając ją na zewnątrz, tym samym oczyszczając się.
Autofagia może mieć znaczenie zarówno pozytywne jak i negatywne. Pozytywna jest wówczas, gdy mitochondrium, będąc w umiarkowany sposób przepuszczalne, pozbywa się śmieci, które mu przeszkadzają, co wiąże się z wydłużeniem życia organizmu. Negatywna, gdy przepuszczalność mitochondrium jest zbyt duża. Badacze udowodnili jednak, że ta zbyt duża przepuszczalność, w pewnych warunkach, też odgrywa ważną rolę zdrowotną.
Naukowcy zaczęli od przeglądu literatury, gdyż już wcześniej było wiadomo, że mutacja i spowodowana przez nią blokada ścieżki sygnałowej mTORC2 oraz białka SGK-1 zwiększa autofagię i zmniejsza długość życia.
Przepuszczalność i oczyszczanie się mitochondriów są wówczas bardzo nasilone. Można by powiedzieć, że mitochondria oczyszczają się wtedy do upadłego, bez zahamowań.
Prowadząc doświadczenia na nicieniach C. elegans (organizmy przydatne do badań laboratoryjnych), naukowcy doszli do wniosku, że białko SGK-1 reguluje otwarcie mPTP (białka – kanaliku) w błonie mitochondrium. W przypadku nagłych stanów chorobowych, jak np. udar, kanalik szeroko się otwiera i przepuszczalność mitochondrium zwiększa się, a długość życia zmniejsza. Kiedy badacze zahamowali przepuszczalność, czyli autofagię – długość życia nicieni ponownie wydłużyła się.
Później przeprowadzili doświadczenie na myszach i sprawdzali zachowanie kanalika mPTP oraz przepuszczalności mitochondriów u gryzoni z urazem reperfuzyjnym, czyli kiedy przepływ krwi zostaje wznowiony po czasowym niedokrwieniu (np. w urazach mózgu, czy ataku serca). To, co wówczas dzieje się w komórkach jest dla nich szokiem. Niedokrwienie może doprowadzić do ich śmierci i uszkodzenia tkanki. Wznowienie krążenia może zaś skutkować w nasileniu tych zjawisk. Amerykanie badając myszy ze zmutowaną wersją genu SGK-1 odkryli, że gryzonie z nasiloną autofagią lepiej zniosły przywrócenie dopływu krwi, co jak sądzą naukowcy świadczy o tym, że w późniejszych etapach urazu reperfuzyjnego, duża przepuszczalność ogranicza zniszczenia tkanki, bo mitochondria, działając jak filterki, mogą pozbyć się nadmiaru nagromadzonej a zbędnej zawartości.
Według badaczy regulacja przepuszczalności mitochondriów poprzez oddziaływanie na ścieżkę sygnałową mTORC2 ma wpływ nie tylko na samą długość życia, ale może być pomocna w leczeniu ataków serca, udarów, kiedy dochodzi do przerwania a następnie wznowienia dopływu krwi do tkanki.
https://nowinkimedyczne.pl/nieszczelnosc-mitochondriow-a-dlugosc-zycia/

"Pomnik - Centrum Zdrowia Dziecka"
w Warszawie

im. Marii Skłodowskiej-Curie
Państwowy Instytut Badawczy

im. prof. dr hab. med. Eleonory Reicher
ul. Spartańska 1, Warszawa

Profilaktyki Zdrowotnej
www.ncpz.eu
Kardiologii
ul. Alpejska 42, 04-628 Warszawa

Warszawskiego Uniwersytetu Medycznego
ul. Banacha 1A, 02-097 Warszawa

Szpital Specjalistyczny
w Warszawie
ul. Bursztynowa 2,
04-749 Warszawa

Zakładów Opieki Zdrowotnej
w Ostrowi Mazowieckiej
ul. Duboisa 68, 07-300 Ostrów Mazowiecka

Zespół Opieki Zdrowotnej
w Mińsku Mazowieckim

im. Bitwy Warszawskiej 1920
w Radzyminie
ul. Konstytucji 3-go Maja 17
05-250 Radzymin

Wojewódzki w Ciechanowie
Powstańców Wielkopolskich 2
06-400 Ciechanów

p.w. Przemienienia Pańskiego
Sp. z o.o.
Aleja Solidarności 67, Warszawa

im. dr Anny Gostyńskiej
Samodzielny Publiczny Zakład Opieki Zdrowotnej
ul. Kasprzaka 17, Warszawa
Szpital Południowy
ul. Rotmistrza Witolda Pileckiego 99, Warszawa

ul. Batalionów Chłopskich 3/7,
96-500 Sochaczew
im. św. Jana Pawła II w Siedlcach
Sp. z o.o.
Księcia Józefa Poniatowskiego 26,
08-110 Siedlce
w Siedlcach
ul. Starowiejska 15, Siedlce

w Garwolinie
ul. Lubelska 50,
08-400 Garwolin

Kliniczny im. prof. Orłowskiego
CMKP
ul. Czerniakowska 231,
00-416 Warszawa

Sp. z o. o.
ul. Stępińska 19/25, Warszawa

ul. Kondratowicza 8, Warszawa

Szpital Kliniczny
im. prof. Adama Grucy
CMKP
ul. Konarskiego 13, Otwock

im. Świętej Rodziny
Madalińskiego 25, 02-544 Warszawa

im. dr med. Włodzimierza Roeflera
w Pruszkowie

w Piasecznie
Adama Mickiewicza 39,
05-500 Piaseczno

Leczenia Chorób Płuc i Gruźlicy
w Otwocku
Reymonta 83/91, 05-400 Otwock

im. prof. dr. med. Jana Bogdanowicza
Samodzielny Publiczny Zakład Opieki Zdrowotnej
ul. Niekłańska 4/24, Warszawa

Szpital Wojewódzki
Drewnica Sp. z o.o.
Rychlińskiego 1, Ząbki

Nieustającej Pomocy
w Wołominie
ul. Gdyńska 1/3
05-200 Wołomin

Neuropsychiatrii Sp. z o.o.
Zagórze k/Warszawy
05-462 Wiązowna

Pogotowia Ratunkowego
i Transportu Sanitarnego
"MEDITRANS"
SPZOZ w Warszawie
ul. Hoża 56, 00-685 Warszawa

U Lekarzy
Przychodnia Bemowo
ul. Bolkowska 2D lok. H2/H3,
01-466 Warszawa

Zakładów Lecznictwa Otwartego
Warszawa-Ochota
ul. Szcześliwicka 36, 02-353 Warszawa

Zakładów Lecznictwa Otwartego Warszawa Bemowo-Włochy
ul. Gen. M. C. Coopera 5, Warszawa

Warszawa-Mokotów
ul. A.J.Madalińskiego 13, Warszawa

im. Dzieci Warszawy
w Dziekanowie Leśnym

GRUPA ZDROWIE

Centrum Medyczne
ul. Miodowa 2
Nowy Dwór Mazowiecki

Państwowy Instytut Badawczy

Kompleksowej Rehabilitacji
Konstancin Jeziorna

ul. Sportowa 30
05 – 090 Raszyn

Opiekuńczo-Lecznicze
Sp. z o.o.
ul. Mehoffera 72/74, Warszawa

Zakład Leczniczo - Rehabilitacyjny
WIGOR
w Legionowie

ul. Bobrowiecka 9, Warszawa
Centrum Diagnostyki Obrazowej
ul.Bobrowiecka 9, Warszawa
Sióstr Felicjanek
im. bł. Hanny Chrzanowskiej
ul. Nowowiejska 10A, Warszawa

ul. Piłsudskiego 3a
05-510 Konstancin-Jeziorna

Bezpieczny Dom Opieki
ul.Bobrowiecka 9, Warszawa

Odzyskać Radość
Bogurzyn 87, 06-521 Wiśniewo

Ale Frajda
ul. Bolesławicka 40, Warszawa

Sprzętu Ortopedycznego S.A.
al. Bohaterów Września 9, Warszawa


Usług Dydaktycznych
ul. Rymanowska 15a
35-083 Rzeszów
im. Tadeusza Koźluka
ul. Bobrowiecka 9, 00-728 Warszawa
INFORMACJE O UCZELNI / REKRUTACJA: więcej w zakładce KONTAKT
-
-
e.REKRUTACJA
-





